Bạn đã bao giờ tự hỏi, điều gì khiến chiếc xe đạp của bạn bị gỉ sét, hay tại sao các nhà máy lại cần đến những quy trình phức tạp để làm sạch nước thải? Câu trả lời có thể nằm ở những "anh hùng thầm lặng" trong thế giới hóa học: chất khử. Chúng đóng vai trò then chốt trong vô số phản ứng, từ những quá trình tự nhiên diễn ra hàng ngày đến các ứng dụng công nghiệp tiên tiến. Vậy, chất khử thực sự là gì? Chúng hoạt động ra sao và có tầm quan trọng như thế nào? Hãy cùng nhau khám phá!
Chất Khử Là Gì? "Cho" Đi Là Còn Mãi!
Chắc hẳn bạn đã từng nghe đến phản ứng oxi hóa khử, một trong những phản ứng quan trọng nhất trong hóa học. Vậy chất khử đóng vai trò gì trong "vở kịch" này?
Nói một cách đơn giản, chất khử là "người hùng" sẵn sàng nhường electron cho chất khác trong phản ứng. Hành động "cho đi" này không hề vô nghĩa, mà nó giúp chất khác "lên đời" – tức là bị khử (giảm số oxi hóa).

Vậy bản chất của chất khử là gì?
- Nhường electron: Đây là đặc điểm nổi bật nhất. Chất khử có "khả năng" cho đi electron để ổn định cấu hình electron của mình.
- Số oxi hóa tăng: Khi nhường electron, số oxi hóa của chất khử sẽ tăng lên. Ví dụ, kim loại natri (Na) có số oxi hóa là 0, khi tham gia phản ứng và nhường electron, nó sẽ trở thành ion natri (Na+) với số oxi hóa là +1.
- Bị oxi hóa: Vì nhường electron cho chất khác, nên bản thân chất khử sẽ bị oxi hóa.
Ví dụ dễ hiểu:
Hãy tưởng tượng bạn có một chiếc kẹo và bạn cho bạn của mình chiếc kẹo đó. Bạn chính là chất khử (cho đi kẹo = cho đi electron), và bạn của bạn là chất oxi hóa (nhận kẹo = nhận electron). Sau khi cho kẹo, bạn "mất" kẹo (bị oxi hóa), còn bạn của bạn "có" kẹo (bị khử).
Tóm lại: Chất khử là "nhân vật" quan trọng trong phản ứng oxi hóa khử, sẵn sàng "cho đi" electron để giúp chất khác "thăng hoa". Quá trình này làm thay đổi số oxi hóa của cả chất khử và chất oxi hóa, tạo nên những biến đổi hóa học kỳ diệu.
Chất Khử – "Nhân Tố Bí Ẩn" Của Phản Ứng Oxi Hóa Khử
Trong thế giới hóa học đầy thú vị, phản ứng oxi hóa khử đóng vai trò then chốt, và chất khử chính là "người hùng" thầm lặng. Vậy, chất khử có vai trò quan trọng đến mức nào?
Chất khử là "người cho đi" electron, sẵn sàng nhường electron cho chất khác. Quá trình này không chỉ đơn thuần là trao đổi, mà còn là chìa khóa để khởi động và duy trì nhiều phản ứng hóa học quan trọng.
- Cung cấp electron: Chất khử là nguồn cung cấp electron dồi dào, giúp các chất khác "giàu có" hơn về mặt điện tích âm.
- Bị oxi hóa: Khi nhường electron, bản thân chất khử lại bị oxi hóa, số oxi hóa tăng lên. Đây là một quy luật tất yếu trong phản ứng oxi hóa khử.
- "Chống lưng" cho ăn mòn điện hóa: Trong quá trình ăn mòn kim loại, chất khử đóng vai trò quan trọng trong việc tạo ra dòng điện, thúc đẩy quá trình phá hủy vật liệu. Ví dụ, kẽm thường được dùng làm chất khử để bảo vệ sắt khỏi bị ăn mòn.
Tầm quan trọng của chất khử không chỉ giới hạn trong phòng thí nghiệm. Chúng ta bắt gặp vai trò của chúng ở khắp mọi nơi:
- Sản xuất công nghiệp: Trong luyện kim, chất khử giúp tách kim loại từ quặng.
- Pin và ắc quy: Chất khử là thành phần không thể thiếu, cung cấp electron để tạo ra dòng điện.
- Xử lý nước thải: Chất khử được sử dụng để loại bỏ các chất ô nhiễm, làm sạch nguồn nước.
Tóm lại, chất khử là một "nhân tố bí ẩn" nhưng vô cùng quan trọng trong phản ứng oxi hóa khử. Khả năng nhường electron của chúng không chỉ thúc đẩy các phản ứng hóa học, mà còn đóng góp vào nhiều ứng dụng thực tiễn trong đời sống và công nghiệp.

"Điểm Danh" Tính Chất Cốt Lõi Của Chất Khử
Chất khử không chỉ là những "người hùng thầm lặng" trong thế giới hóa học, mà còn sở hữu những đặc điểm và tính chất vô cùng thú vị. Cùng khám phá xem "nhân vật" này có gì đặc biệt nhé!
-
Khả năng "cho đi" electron: Đây chính là "siêu năng lực" của chất khử. Chúng sẵn sàng nhường electron cho chất khác trong phản ứng, giúp chất kia "lên đời" bằng cách giảm số oxi hóa.
-
Số oxi hóa "thấp bé nhẹ cân": Thông thường, chất khử có số oxi hóa thấp, hoặc đang ở mức thấp nhất có thể. Điều này tạo điều kiện thuận lợi để chúng "bung lụa" khả năng nhường electron.
-
Tính chất vật lý đa dạng: Chất khử có thể tồn tại ở nhiều trạng thái khác nhau:
- Kim loại: Như kẽm (Zn), sắt (Fe) – những "chiến binh" quen thuộc trong các phản ứng oxi hóa khử.
- Phi kim: Ví dụ như hydro (H₂) – "người bạn" của các phản ứng khử trong công nghiệp.
- Hợp chất: Ví dụ như axit oxalic (H₂C₂O₄) – một chất khử mạnh mẽ trong phòng thí nghiệm.
-
"Máu chiến" trong phản ứng: Chất khử rất "hăng hái" tham gia vào các phản ứng hóa học, đặc biệt là các phản ứng oxi hóa khử. Chúng có thể khử các ion kim loại, phi kim, hoặc thậm chí cả các hợp chất hữu cơ.
- Ví dụ, trong quá trình luyện gang, carbon (C) đóng vai trò chất khử, "cướp" oxi từ oxit sắt (Fe₂O₃) để tạo ra sắt (Fe) nguyên chất.
-
Tính khử mạnh yếu khác nhau: Không phải chất khử nào cũng "khỏe" như nhau. Có những chất khử mạnh, dễ dàng nhường electron, nhưng cũng có những chất khử yếu hơn, cần điều kiện "kích hoạt" mới phát huy được khả năng.
Hiểu rõ những đặc điểm và tính chất này sẽ giúp bạn dễ dàng nhận diện và sử dụng chất khử một cách hiệu quả trong học tập và ứng dụng thực tế.

Chất Khử "Biến Hình": Đâu Là Sự Khác Biệt?
Chất khử không chỉ đơn thuần là những "người hùng" thầm lặng nhường electron. Thế giới của chúng còn đa dạng hơn bạn tưởng! Bạn đã bao giờ tự hỏi, vì sao vitamin C (một chất khử hữu cơ) lại giúp tăng cường hệ miễn dịch, còn kẽm (một chất khử vô cơ) lại có mặt trong pin? Để vén màn bí mật này, chúng ta sẽ cùng nhau khám phá thế giới song hành của chất khử hữu cơ và vô cơ, từ cấu trúc phức tạp đến những ứng dụng "đỉnh của chóp" trong cuộc sống hàng ngày.
"Anh Hùng" Thầm Lặng Trong Thế Giới Hữu Cơ – Chất Khử
Chất khử hữu cơ, nghe có vẻ "cao siêu", nhưng thực ra lại đóng vai trò cực kỳ quan trọng trong cuộc sống của chúng ta, từ những phản ứng sinh hóa diễn ra trong cơ thể đến các quy trình công nghiệp phức tạp. Vậy, "anh hùng" này có gì đặc biệt?
Cấu Trúc "Linh Hoạt"
Khác với chất khử vô cơ thường có cấu trúc đơn giản, chất khử hữu cơ sở hữu cấu trúc phức tạp hơn nhiều, được tạo thành từ các nguyên tử carbon liên kết với hydro, oxy, nitơ… Sự đa dạng này cho phép chúng tham gia vào vô số các phản ứng khác nhau. Hãy tưởng tượng chúng như những "bàn tay" với nhiều ngón, có thể "nắm" và "thả" electron một cách linh hoạt.
Tính Chất "Biến Hóa"
Tính chất của chất khử hữu cơ phụ thuộc rất nhiều vào cấu trúc phân tử của chúng. Một số chất khử hữu cơ dễ dàng nhường electron, trong khi những chất khác lại "kén chọn" hơn. Điều này cho phép các nhà khoa học và kỹ sư "thiết kế" các chất khử hữu cơ phù hợp với từng ứng dụng cụ thể.
Vai Trò "Không Thể Thiếu"
-
Trong cơ thể sống: Vitamin C (axit ascorbic) là một ví dụ điển hình. Nó hoạt động như một chất khử, bảo vệ tế bào khỏi các gốc tự do gây hại, giúp tăng cường hệ miễn dịch và duy trì làn da khỏe mạnh.
-
Trong công nghiệp: Các chất khử hữu cơ được sử dụng rộng rãi trong quá trình sản xuất thuốc nhuộm, nhựa, dược phẩm và nhiều sản phẩm khác. Ví dụ, các hợp chất aldehyde được sử dụng để khử các ion kim loại trong quá trình xử lý nước thải.
-
Trong quá trình sinh học: NADH và FADH2 là hai chất khử hữu cơ quan trọng tham gia vào chuỗi vận chuyển electron trong hô hấp tế bào, cung cấp năng lượng cho cơ thể hoạt động.
Tóm lại, chất khử hữu cơ là những "chiến binh" thầm lặng nhưng vô cùng quan trọng, góp phần vào sự sống và sự phát triển của xã hội. Việc nghiên cứu và ứng dụng chúng một cách hiệu quả sẽ mang lại nhiều lợi ích to lớn cho nhân loại.

"Anh Hùng" Thầm Lặng Trong Phản Ứng – Chất Khử Vô Cơ
Chất khử vô cơ, những "anh hùng" thầm lặng trong thế giới hóa học, đóng vai trò then chốt trong vô số phản ứng và quy trình công nghiệp. Khác với đồng nghiệp hữu cơ, chúng thường là các nguyên tố kim loại, ion hoặc hợp chất đơn giản hơn, nhưng sức mạnh khử của chúng thì không hề kém cạnh.
Đặc Điểm Nhận Diện
- "Cho Đi" Electron: Điểm mấu chốt của chất khử vô cơ là khả năng "cho đi" electron cho chất khác. Quá trình này làm tăng số oxi hóa của chính nó.
- Đa Dạng "Ngoại Hình": Chúng có thể là kim loại (như natri, kẽm), phi kim (như hydro), hoặc các ion (như ion sắt (II)).
- Phản Ứng Mạnh Mẽ: Nhiều chất khử vô cơ phản ứng rất mạnh, thậm chí có thể gây nổ nếu không được xử lý cẩn thận.
Ứng Dụng "Siêu To Khổng Lồ"
- Luyện Kim: Trong ngành luyện kim, chất khử vô cơ như carbon (than cốc) được sử dụng để tách kim loại từ quặng. Ví dụ, trong lò cao, carbon khử oxit sắt thành sắt kim loại.
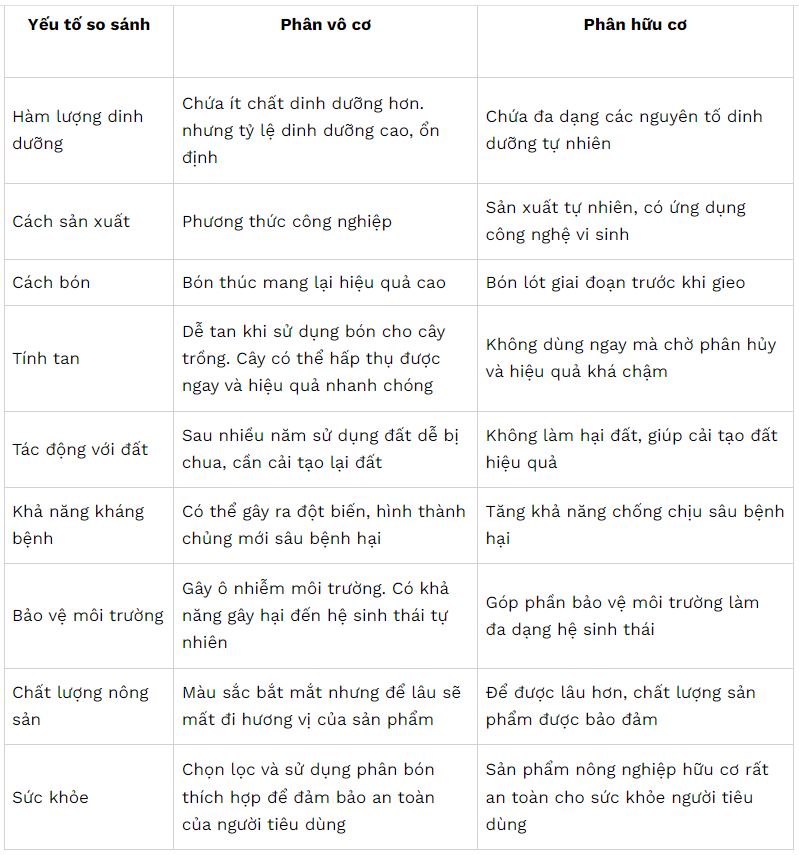
- Sản Xuất Phân Bón: Amoniac (NH3), một chất khử vô cơ quan trọng, là nguyên liệu chính để sản xuất phân bón, giúp tăng năng suất cây trồng.
- Xử Lý Nước: Các chất khử như natri sunfit (Na2SO3) được sử dụng để loại bỏ clo dư trong nước thải, bảo vệ môi trường.
- Pin và Ắc Quy: Kim loại kẽm (Zn) là một chất khử quan trọng trong pin và ắc quy, cung cấp electron để tạo ra dòng điện.
- Công Nghiệp Hóa Chất: Hydro (H2) được sử dụng rộng rãi trong công nghiệp hóa chất để khử các hợp chất hữu cơ, ví dụ như trong quá trình hydro hóa dầu thực vật để sản xuất bơ thực vật.
Ví Dụ Điển Hình
- Natri (Na): Kim loại kiềm này là một chất khử cực mạnh, được sử dụng trong nhiều phản ứng tổng hợp hữu cơ và vô cơ.
- Kẽm (Zn): Được sử dụng rộng rãi trong pin, mạ kim loại và sản xuất hợp kim.
- Hydro (H2): Chất khử quan trọng trong công nghiệp hóa chất, luyện kim và sản xuất năng lượng.
- Sắt (II) clorua (FeCl2): Được sử dụng trong xử lý nước thải và làm chất khử trong phòng thí nghiệm.
Chất khử vô cơ không chỉ là những hóa chất đơn thuần; chúng là những tác nhân quan trọng thúc đẩy nhiều quy trình thiết yếu trong đời sống và công nghiệp, góp phần vào sự phát triển của xã hội hiện đại.

Bắt "Tên" Chất Khử Trong Phản Ứng Hóa Học
Bạn đang "vật lộn" với việc tìm chất khử trong một "rừng" phương trình hóa học? Đừng lo, việc này không hề khó như bạn nghĩ đâu! Chỉ cần nắm vững vài "bí kíp" sau, bạn sẽ "bắt" được chất khử ngay lập tức.
Bước 1: "Soi" Số Oxi Hóa
Đây là bước quan trọng nhất! Hãy nhớ rằng:
- Chất khử là "anh chàng" nhường electron, và số oxi hóa của "anh ta" sẽ tăng lên sau phản ứng.
- Chất oxi hóa là "người" nhận electron, và số oxi hóa của "người đó" sẽ giảm xuống sau phản ứng.
Ví dụ, xét phản ứng đơn giản sau:
Zn + Cu2+ -> Zn2+ + Cu
- Số oxi hóa của Zn tăng từ 0 lên +2 (Zn nhường electron).
- Số oxi hóa của Cu giảm từ +2 xuống 0 (Cu nhận electron).
Vậy, Zn chính là chất khử trong phản ứng này!
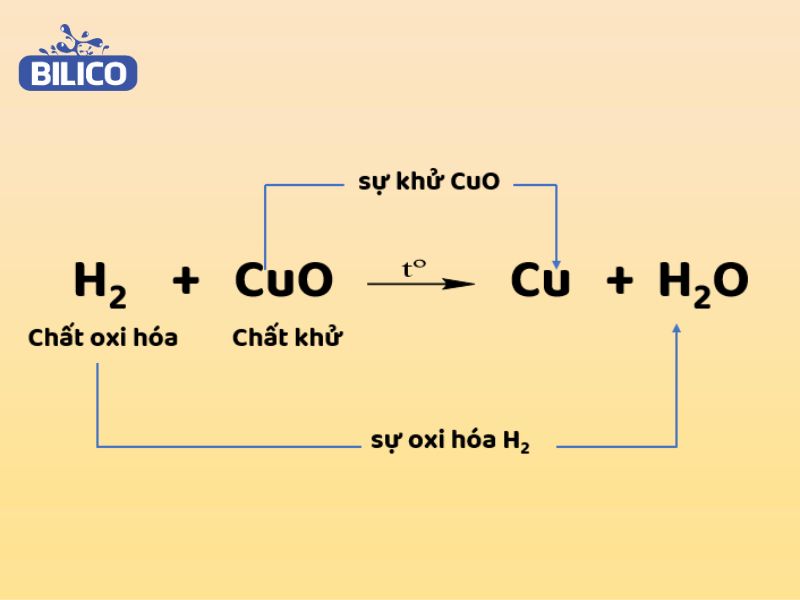
Bước 2: Viết Quá Trình Oxi Hóa và Khử
Viết quá trình giúp bạn hình dung rõ ràng hơn sự di chuyển của electron.
- Quá trình oxi hóa (của chất khử): Zn → Zn2+ + 2e
- Quá trình khử (của chất oxi hóa): Cu2+ + 2e → Cu
Nhìn vào quá trình oxi hóa, bạn thấy Zn "cho đi" 2 electron. Điều này khẳng định Zn là chất khử.
Bước 3: Nhận Diện "Gương Mặt" Chất Khử
Một số "gương mặt" chất khử thường gặp bạn nên "nhớ mặt":
- Kim loại: Hầu hết kim loại đều có tính khử (dễ nhường electron). Ví dụ: Na, K, Mg, Al, Fe,…
- Các hợp chất có số oxi hóa thấp: Ví dụ: H2S (lưu huỳnh có số oxi hóa -2), FeO (sắt có số oxi hóa +2),…
- Một số ion âm: Ví dụ: I- (ion iodua), SO32- (ion sulfit),…
Lưu ý: Không phải lúc nào cũng "nhìn mặt mà bắt hình dong" được. Hãy luôn kiểm tra số oxi hóa để chắc chắn!
Mẹo Nhỏ "Bỏ Túi"
- "Khử tăng, Oxi giảm": Một câu "thần chú" giúp bạn nhớ nhanh.
- Luyện tập thường xuyên: Càng làm nhiều bài tập, bạn càng "nhạy bén" trong việc nhận diện chất khử.
Chúc bạn thành công trên con đường chinh phục hóa học!
Chất Khử "Xâm Nhập" Đời Sống – Bạn Có Biết?
Chất khử không chỉ là "người hùng thầm lặng" trong phòng thí nghiệm đâu nhé! Chúng len lỏi vào cuộc sống hàng ngày và cả các ngành công nghiệp lớn, đóng vai trò quan trọng mà có thể bạn chưa hề hay biết. Cùng khám phá những ứng dụng "bá đạo" của chất khử nào!
Hóa Học – "Phù Thủy" Biến Hóa
Trong hóa học, chất khử là "trợ thủ đắc lực" giúp tạo ra vô vàn hợp chất mới. Ví dụ, hydro (H₂) được dùng để khử các oxit kim loại thành kim loại nguyên chất. Quá trình này quan trọng trong sản xuất thép, nhôm và nhiều kim loại khác.
Công Nghiệp – "Cỗ Máy" Sản Xuất
- Sản xuất giấy: Natri hydrosulfit (Na₂S₂O₄) là "cứu tinh" giúp tẩy trắng bột giấy, cho ra những trang giấy trắng tinh mà chúng ta vẫn dùng hàng ngày.
- Dệt nhuộm: Chất khử giúp loại bỏ màu không mong muốn trên vải, chuẩn bị cho quá trình nhuộm màu mới.
Môi Trường – "Chiến Binh" Xanh
Chất khử tham gia vào quá trình xử lý nước thải, loại bỏ các chất ô nhiễm như clo dư thừa, các ion kim loại nặng, giúp trả lại nguồn nước sạch cho môi trường.
Dược Phẩm – "Thần Dược" Cứu Người
- Tổng hợp thuốc: Nhiều loại thuốc được tổng hợp nhờ các phản ứng khử. Ví dụ, vitamin C (axit ascorbic) là một chất khử mạnh, đóng vai trò quan trọng trong nhiều phản ứng sinh hóa trong cơ thể.
- Bảo quản thuốc: Chất khử giúp ngăn chặn quá trình oxy hóa, kéo dài thời gian sử dụng của thuốc.
Thực Phẩm – "Vệ Sĩ" An Toàn
- Bảo quản thực phẩm: Axit ascorbic (vitamin C) và sulfit được sử dụng để ngăn chặn quá trình oxy hóa, giữ cho thực phẩm tươi ngon lâu hơn.
- Sản xuất đường: Lưu huỳnh đioxit (SO₂) được dùng để tẩy màu trong quá trình sản xuất đường, giúp đường có màu trắng tinh.
Năng Lượng – "Nguồn Sống" Tương Lai
Trong pin nhiên liệu, chất khử (thường là hydro) phản ứng với chất oxy hóa (thường là oxy) để tạo ra điện năng. Đây là một nguồn năng lượng sạch và bền vững, hứa hẹn sẽ thay thế các nguồn năng lượng hóa thạch trong tương lai.

An Toàn Là Bạn: Mẹo Dùng Chất Khử "Chuẩn Không Cần Chỉnh"
Chất khử "mạnh mẽ" là thế, nhưng nếu không "chơi" đúng cách thì "toang" đấy nhé! Dưới đây là những "bí kíp" bỏ túi giúp bạn dùng chất khử an toàn, hiệu quả, lại còn bảo vệ môi trường nữa chứ!
Chọn Mặt Gửi Vàng: "Chất Khử" Nào Phù Hợp?
Không phải cứ chất khử nào cũng "cân" được mọi loại phản ứng đâu nha. Hãy "soi" kỹ thông tin sản phẩm, xem nó có "hợp cạ" với mục đích sử dụng của bạn không. Ví dụ, khử trùng nước sinh hoạt thì dùng loại khác, còn tẩy trắng quần áo thì lại là "em" khác nữa.
"Thở Oxy" Cho Không Gian: Thông Gió Cực Quan Trọng
Chất khử đôi khi "nhả" ra những "bé" khí không mấy dễ chịu, thậm chí có thể gây hại. Vì vậy, hãy đảm bảo không gian làm việc luôn thoáng đãng, "gió lùa" vi vu nhé. Nếu "bí" quá thì "tậu" ngay một em quạt thông gió là "chuẩn bài".
"Giáp Sắt" Bảo Vệ: Đồ Bảo Hộ Cá Nhân "Must-Have"
Đừng chủ quan nghĩ rằng "chắc không sao đâu". Găng tay, kính bảo hộ, khẩu trang… là những "vũ khí" lợi hại giúp bạn tránh khỏi những "tai nạn nghề nghiệp" không đáng có. "Cẩn tắc vô áy náy" mà!
"Dọn Dẹp Chiến Trường": Làm Sạch Sau Khử Trùng
Sau khi "xử lý" xong, đừng quên "tổng vệ sinh" khu vực làm việc nhé. Lau chùi kỹ càng giúp loại bỏ cặn chất khử còn sót lại, đảm bảo an toàn cho mọi người xung quanh.
"Xử Lý" Rác Thải: Đúng Quy Trình, "Xanh" Môi Trường
Chất thải từ chất khử không phải loại rác "tầm thường" đâu nha. Hãy tìm hiểu kỹ quy định của địa phương về cách xử lý rác thải hóa chất, hoặc liên hệ với các đơn vị chuyên xử lý để được hỗ trợ.
"Liều Lượng Là Vàng": Đừng "Quá Tay"
"Tham thì thâm" – câu này đúng trong mọi trường hợp, kể cả khi sử dụng chất khử. Dùng đúng liều lượng khuyến cáo không chỉ giúp bạn đạt hiệu quả tốt nhất mà còn tránh được những tác dụng phụ không mong muốn.
Nhớ kỹ những "bí kíp" này, bạn sẽ trở thành một "cao thủ" sử dụng chất khử an toàn, hiệu quả, lại còn góp phần bảo vệ sức khỏe và môi trường nữa chứ!

