Nhìn quanh bạn xem, không khí bạn hít thở, nước bạn uống, thậm chí cả cấu tạo cơ thể chúng ta – tất cả đều phụ thuộc vào một nhóm nguyên tố thường "kín đáo" hơn so với những kim loại lấp lánh. Đó chính là phi kim. Dù không phô trương như vàng bạc, vai trò của chúng lại cực kỳ to lớn và không thể thay thế trong mọi mặt đời sống. Bạn có bao giờ tự hỏi, điều gì làm nên sự khác biệt cốt lõi giữa phi kim và kim loại? Tính chất nào khiến chúng phản ứng theo những cách độc đáo, và làm thế nào mà những nguyên tố tưởng chừng đơn giản như Oxi hay Carbon lại trở thành nền tảng cho vô số ứng dụng từ y tế đến công nghiệp? Hãy cùng nhau vén màn bí ẩn, khám phá thế giới phi kim từ định nghĩa cơ bản nhất, đi sâu vào tính chất đặc trưng về vật lý, những phản ứng hóa học đa dạng, cách phân loại, và cuối cùng là nhìn nhận tầm quan trọng không thể thiếu của chúng trong cuộc sống hiện đại.
Phi kim là gì Sao khác Kim loại
Nếu kim loại thường làm ta liên tưởng đến sự sáng bóng, cứng cáp và dẫn điện ‘ro ro’, thì phi kim lại có một thế giới riêng biệt, đôi khi ‘ẩn mình’ hơn một chút. Đơn giản nhất, phi kim là những nguyên tố hóa học không phải là kim loại. Nghe có vẻ hiển nhiên nhỉ? Nhưng sự khác biệt giữa hai nhóm này lại là nền tảng để hiểu rất nhiều điều thú vị trong hóa học.

Trong bảng tuần hoàn quen thuộc, phi kim thường ‘ngồi’ ở phía bên phải, tách biệt với phần lớn các nguyên tố kim loại bởi một đường ranh giới hình bậc thang (trừ Hydro là phi kim nhưng lại nằm ở nhóm IA). Số lượng phi kim ít hơn kim loại rất nhiều, nhưng vai trò của chúng trong tự nhiên và đời sống lại cực kỳ quan trọng.
Khác biệt lớn nhất nằm ngay trong ‘tâm hồn’ của nguyên tử – cấu trúc electron lớp ngoài cùng. Nếu kim loại có xu hướng dễ dàng ‘cho đi’ các electron hóa trị để trở thành ion dương (cation), thì phi kim lại có ‘tính cách’ ngược lại. Chúng thường có nhiều electron ở lớp ngoài cùng và rất ‘thích’ nhận thêm electron từ nguyên tử khác để đạt được cấu hình electron bền vững giống khí hiếm. Khi nhận electron, phi kim sẽ biến thành ion âm (anion). Chính cái xu hướng nhận electron này quyết định nhiều tính chất đặc trưng của phi kim.
Một điểm khác biệt dễ thấy bằng mắt thường (hoặc qua thí nghiệm) là khả năng dẫn điện và dẫn nhiệt. Nhắc đến kim loại là nghĩ ngay đến dây điện, nồi niêu xoong chảo… vì chúng dẫn điện, dẫn nhiệt cực tốt. Còn phi kim thì sao? Hầu hết là ‘người dẫn đường’ rất tệ cho dòng điện hay hơi nóng. Nguyên nhân là vì các electron hóa trị trong phi kim bị giữ chặt bởi hạt nhân, không có electron tự do di chuyển như trong kim loại. Than chì (một dạng thù hình của carbon) là một trong số ít phi kim có khả năng dẫn điện đáng kể, nhưng đó là trường hợp ngoại lệ.
Độ âm điện cũng là một thước đo quan trọng để phân biệt. Độ âm điện là khả năng hút electron về phía mình khi tạo liên kết hóa học. Phi kim có độ âm điện cao, thể hiện rõ cái ‘tính cách’ thích kéo electron về phía mình. Ngược lại, kim loại có độ âm điện thấp. Chính sự chênh lệch về độ âm điện giữa kim loại và phi kim khi kết hợp với nhau sẽ tạo nên những liên kết ion đặc trưng.
Tóm lại, phi kim và kim loại như hai thái cực trong thế giới nguyên tố, khác nhau từ cách ‘cư xử’ của electron đến những tính chất vật lý, hóa học cơ bản nhất như khả năng dẫn điện, dẫn nhiệt hay độ âm điện. Hiểu rõ những khác biệt cốt lõi này sẽ giúp chúng ta ‘giải mã’ được vô vàn phản ứng và ứng dụng của chúng trong cuộc sống.
Phi kim Có Vẻ Ngoài Ra Sao
Nhìn bề ngoài, thế giới phi kim thật đa dạng, chẳng tuân theo một khuôn mẫu cố định nào cả. Ở nhiệt độ phòng, bạn có thể thấy chúng tồn tại dưới đủ ba trạng thái quen thuộc: rắn, lỏng, và khí. Chẳng hạn, lưu huỳnh hay carbon là những anh chàng rắn rỏi, brom lại lỏng lẻo như nước, còn oxi hay nitơ thì bay bổng như khí trời vậy đó. Sự đa dạng này tạo nên bức tranh muôn màu muôn vẻ cho nhóm nguyên tố đặc biệt này.
Khác với vẻ bóng bẩy, dễ dát mỏng hay kéo sợi của kim loại, phi kim thường có vẻ ngoài khá… khiêm tốn. Phi kim rắn thường giòn, dễ vỡ vụn khi chịu tác động. Thử lấy búa đập vào một mẩu lưu huỳnh xem, nó sẽ tan tành ngay chứ chẳng dẹp lép như miếng nhôm đâu.
Một điểm đặc trưng nữa khiến phi kim khác biệt hẳn là khả năng dẫn điện và dẫn nhiệt. Hầu hết phi kim là những kẻ cách ly tài tình. Chúng dẫn điện và dẫn nhiệt rất kém. Nghĩ mà xem, dây điện nhà mình làm bằng đồng (kim loại) chứ có ai dùng lưu huỳnh hay phốt pho đâu, đúng không nào? Tính chất này làm cho chúng trở thành vật liệu lý tưởng cho nhiều ứng dụng cần cách điện, cách nhiệt.
Nhiệt độ nóng chảy và nhiệt độ sôi của phi kim nhìn chung là khá thấp. Điều này giải thích vì sao nhiều phi kim tồn tại ở trạng thái lỏng hoặc khí ngay trong điều kiện thường. Chỉ một số ít phi kim rắn như carbon (dạng kim cương) mới có nhiệt độ nóng chảy cực cao, nhưng đó là trường hợp ngoại lệ đặc biệt.
Tóm lại, phi kim không có vẻ ngoài hào nhoáng hay tính chất vật lý đồng nhất như kim loại. Chúng đa dạng về trạng thái, giòn (nếu là rắn), dẫn điện/nhiệt kém và thường có nhiệt độ nóng chảy, sôi thấp. Chính những đặc điểm này lại mở ra vô vàn ứng dụng thú vị cho chúng trong cuộc sống.
Phi kim Hoạt Động Hóa Học Thế Nào
Nếu như kim loại hào phóng "cho đi" electron, thì phi kim lại cực kỳ "hảo" electron, luôn tìm cách "bắt lấy" từ nguyên tố khác. Chính cái sự "thèm" electron này đã làm nên tính chất hóa học đặc trưng và vô cùng đa dạng của chúng. Bạn biết không, nước mà chúng ta uống hàng ngày chính là kết quả của phản ứng giữa hai phi kim là hydro và oxi đấy! Từ việc kết hợp với kim loại để tạo ra muối ăn quen thuộc, hay "bắt tay" với hydro tạo nên những hợp chất khí đặc trưng, đến việc phản ứng với chính oxi trong không khí, phi kim tham gia vào vô số quá trình hóa học quan trọng. Vậy, bạn có tò mò không, phi kim sẽ "bắt tay" với kim loại, hydro hay chính oxi như thế nào để tạo ra những thứ quanh ta?
Phi Kim Gặp Kim Loại Kết Quả Là Muối Hay Oxit
Khi phi kim "bắt tay" với kim loại, một phản ứng hóa học thú vị thường diễn ra. Cứ hình dung thế này, kim loại thì hào phóng, dễ dàng "cho đi" các electron của mình, còn phi kim lại có xu hướng "nhận về". Hai tính chất đối lập này khi gặp nhau lại tạo nên sự kết hợp rất mạnh mẽ.
Để cuộc "gặp gỡ" này xảy ra, đôi khi cần một chút "xúc tác" từ bên ngoài, mà phổ biến nhất chính là nhiệt độ. Bạn sẽ thấy nhiều phản ứng giữa phi kim và kim loại cần phải đun nóng mới bắt đầu hoặc diễn ra nhanh hơn.
Vậy sản phẩm cuối cùng của "cuộc tình" này là gì? Thường thì đó là muối. Ví dụ kinh điển nhất chính là khi kim loại natri (Na) mềm dẻo gặp khí clo (Cl₂) độc hại, chỉ cần một chút kích thích là bùng cháy và tạo ra muối ăn (NaCl) quen thuộc. Hay như sắt (Fe) khi phản ứng với lưu huỳnh (S) sẽ tạo thành sắt(II) sunfua (FeS), một loại muối.
Tuy nhiên, có một trường hợp đặc biệt. Nếu phi kim tham gia phản ứng là oxi (O₂), sản phẩm tạo thành lại là oxit kim loại. Nghĩa là, khi kim loại kết hợp với oxi, chúng ta sẽ thu được hợp chất của kim loại với oxi. Chẳng hạn, magie (Mg) cháy sáng trong không khí (chứa oxi) tạo ra oxit magie (MgO) màu trắng. Sắt (Fe) bị gỉ sét chính là quá trình nó từ từ phản ứng với oxi và hơi nước trong không khí để tạo thành các loại oxit sắt.
Tóm lại, khi phi kim phản ứng với kim loại, sản phẩm thường là muối, trừ trường hợp phi kim đó là oxi thì sẽ tạo ra oxit kim loại. Điều kiện phản ứng có thể cần nhiệt độ, tùy thuộc vào độ hoạt động của các nguyên tố tham gia.
Khi Phi Kim Kết Hợp Cùng Hydro
Hydro, chàng lãng tử độc hành trong bảng tuần hoàn, lại rất thích "bắt cặp" với các cô nàng phi kim đấy. Tùy vào "tính cách" của từng phi kim mà cuộc gặp gỡ này sẽ diễn ra khác nhau, có khi cần nhiệt độ cao, có khi cần xúc tác, và sản phẩm tạo ra cũng đa dạng lắm. Thường thì, kết quả của màn kết hợp này là những hợp chất ở thể khí, mỗi loại mang một đặc điểm riêng biệt.
Hãy thử nhìn xem vài "cặp đôi" tiêu biểu nhé. Oxi, nàng phi kim hoạt bát, chỉ cần một tia lửa nhỏ là có thể kết hợp ngay với hydro để tạo ra nước (H₂O) – hợp chất quá đỗi quen thuộc và cần thiết cho sự sống. Phản ứng này tỏa nhiệt rất mạnh, cho thấy sự gắn bó bền chặt giữa chúng.
Còn Clo thì sao? Cô nàng halogen này cũng chẳng kém cạnh. Clo phản ứng với hydro tạo ra khí hydro clorua (HCl). Phản ứng này có thể xảy ra ngay ở nhiệt độ thường khi có ánh sáng, nhưng sẽ mạnh mẽ hơn nhiều nếu được đun nóng. Khí HCl tan rất tốt trong nước, tạo thành dung dịch axit clohidric mà chúng ta vẫn hay nghe nói đến.
Lưu huỳnh có vẻ "hiền" hơn một chút. Để lưu huỳnh phản ứng được với hydro, chúng ta cần đun nóng mạnh. Sản phẩm thu được là khí hydro sunfua (H₂S), một loại khí có mùi đặc trưng như trứng thối và khá độc. Điều kiện phản ứng khác nhau cho thấy mức độ "thiện chí" kết hợp của từng phi kim với hydro cũng khác nhau đấy.
Nhìn chung, phản ứng giữa phi kim và hydro là một ví dụ điển hình cho thấy sự đa dạng trong hóa học. Điều kiện phản ứng, từ nhiệt độ, áp suất cho đến sự có mặt của xúc tác, đều đóng vai trò quan trọng trong việc quyết định liệu phản ứng có xảy ra hay không và sản phẩm tạo thành sẽ có tính chất như thế nào. Những hợp chất khí tạo ra từ đây lại mở ra vô vàn ứng dụng khác trong đời sống và công nghiệp.
Khi Phi kim Gặp Oxi
Vậy phi kim phản ứng với oxi thì sao nhỉ? Đây là một "cuộc gặp gỡ" khá phổ biến trong thế giới hóa học đấy. Nhiều anh chàng phi kim rất thích "bắt tay" với oxi, tạo ra những hợp chất đặc biệt. Phản ứng này có thể diễn ra dưới nhiều điều kiện khác nhau, đôi khi cần chút "lửa" (nhiệt độ cao) để khởi động, nhưng cũng có lúc chỉ cần tiếp xúc là đủ.
Khi kết hợp, phi kim và oxi tạo ra các hợp chất gọi là oxit phi kim. Điều thú vị là hầu hết các oxit phi kim này lại có tính chất axit. Nghĩa là, khi chúng tan trong nước, chúng sẽ tạo ra các dung dịch axit tương ứng. Vì thế, người ta hay gọi chúng là oxit axit.
Lấy vài ví dụ cho dễ hình dung nè. Nhớ anh chàng Lưu huỳnh (S) không? Khi đốt Lưu huỳnh trong không khí (chứa oxi), ta thu được khí Lưu huỳnh đioxit (SO2). Khí này chính là một oxit phi kim điển hình. SO2 mà gặp nước, như trong các đám mây chẳng hạn, sẽ tạo thành axit sunfurơ (H2SO3), góp phần không nhỏ vào hiện tượng mưa axit đáng lo ngại.
Rồi Photpho (P) nè, khi cháy trong điều kiện đủ oxi, nó tạo ra Điphotpho pentaoxit (P2O5). Hợp chất rắn màu trắng này có ái lực rất mạnh với nước. Chỉ cần gặp nước là nó phản ứng ngay lập tức, sinh ra axit photphoric (H3PO4) – một axit quan trọng, được dùng nhiều trong sản xuất phân bón hay nước giải khát.
Hay quen thuộc nhất có lẽ là Carbon (C). Khi Carbon cháy hoàn toàn, nó cho ra khí Cacbon đioxit (CO2). CO2 cũng là một oxit phi kim. Nó tan trong nước tạo thành axit cacbonic (H2CO3) yếu thôi, chính là cái làm cho nước giải khát có gas của bạn có vị hơi chua chua đó.
Thấy chưa, phản ứng giữa phi kim và oxi không chỉ đơn thuần là kết hợp hai nguyên tố, mà còn tạo ra cả một nhóm chất có tính axit đặc trưng, đóng vai trò quan trọng (và đôi khi là tác động tiêu cực) trong tự nhiên và đời sống.
Phi kim Chia nhóm thế nào và Ai mạnh nhất
Thế giới phi kim không chỉ có một màu đâu nhé, chúng đa dạng lắm! Để dễ bề "làm quen", người ta thường chia bọn này thành các nhóm dựa trên vị trí trong bảng tuần hoàn và những tính chất đặc trưng riêng.
Đầu tiên phải kể đến hai "gia đình" nổi tiếng nhất: nhóm Halogen và nhóm Khí hiếm. Nhóm Halogen bao gồm Fluor (F), Clo (Cl), Brom (Br), Iot (I) và Astatin (At). Đây là những phi kim cực kỳ "năng động", hay còn gọi là hoạt động hóa học mạnh mẽ. Ngược lại, nhóm Khí hiếm gồm Heli (He), Neon (Ne), Argon (Ar), Kripton (Kr), Xenon (Xe), Radon (Rn) lại là những "anh chàng" cực kỳ "chảnh", gần như không thèm phản ứng với bất cứ ai trong điều kiện thường.
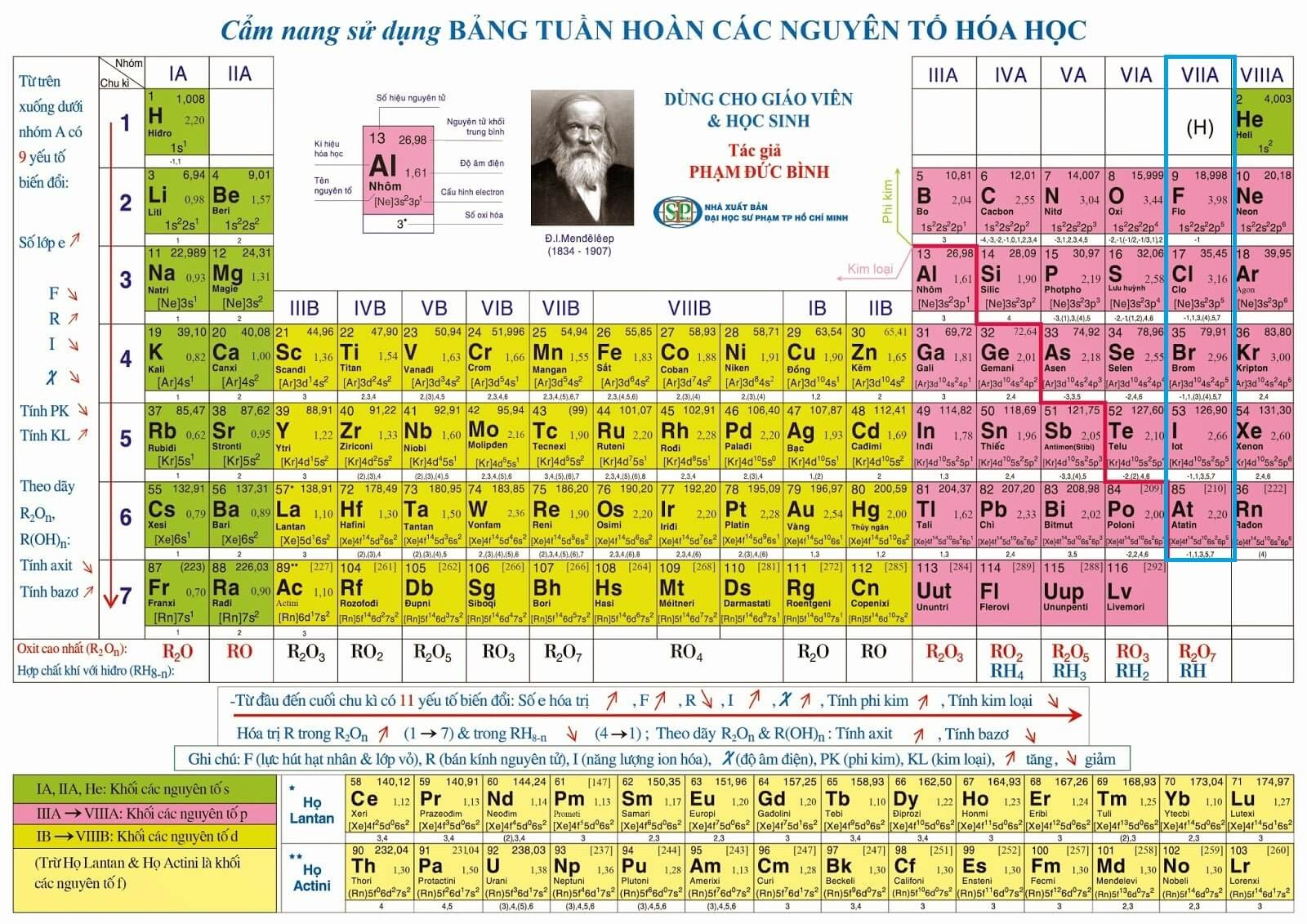
Ngoài ra, còn rất nhiều phi kim khác đứng "lẻ" hoặc thuộc các nhóm khác trong bảng tuần hoàn như Carbon (C), Lưu huỳnh (S), Phosphor (P), Oxi (O), Nitơ (N), Hydro (H), Selen (Se)… Mỗi nguyên tố này lại có "cá tính" và mức độ hoạt động khác nhau, tạo nên sự phong phú cho thế giới phi kim.
Vậy, cái gì quyết định "sức mạnh" hay mức độ hoạt động hóa học của phi kim? Đơn giản thôi, đó là khả năng "giành giật" electron từ nguyên tử khác. Phi kim có xu hướng nhận thêm electron để đạt cấu hình bền vững. Phi kim nào càng "ham hố" nhận electron, thì nó càng hoạt động mạnh.
Chúng ta có thể nhìn vào cách phi kim phản ứng với kim loại hoặc hydro để đánh giá "độ mạnh" của chúng. Phi kim hoạt động mạnh sẽ dễ dàng phản ứng, thậm chí là phản ứng mãnh liệt với kim loại (tạo muối hoặc oxit) và hydro (tạo hợp chất khí). Ví dụ, Fluor là phi kim hoạt động mạnh nhất, nó có thể phản ứng với hầu hết các nguyên tố khác, kể cả một số khí hiếm! Clo cũng rất mạnh, phản ứng nhanh với nhiều kim loại. Càng đi xuống trong nhóm Halogen (từ F đến I), mức độ hoạt động lại giảm dần.
Ngược lại, những phi kim hoạt động yếu hơn sẽ cần điều kiện phản ứng khắc nghiệt hơn hoặc phản ứng xảy ra chậm hơn. Còn các Khí hiếm thì sao? Vì lớp vỏ electron ngoài cùng của chúng đã "đủ đầy" rồi, nên chúng chẳng cần nhận thêm hay cho bớt electron nào cả, đó là lý do chúng gần như không phản ứng và được coi là hoạt động hóa học rất kém.
Tóm lại, việc phân loại giúp chúng ta hệ thống hóa thế giới phi kim đầy màu sắc, còn mức độ hoạt động hóa học lại cho ta biết "tính cách" và khả năng tham gia vào các phản ứng của từng loại phi kim.
Phi kim Những người hùng thầm lặng của đời sống
Nếu kim loại thường được nhắc đến với vẻ ngoài bóng bẩy, cứng cáp, thì phi kim lại là những "người hùng thầm lặng", hiện diện khắp mọi ngóc ngách trong cuộc sống của chúng ta, từ hơi thở hàng ngày đến những sản phẩm công nghệ cao. Vai trò của chúng đa dạng đến mức khó tin, len lỏi vào y tế, công nghiệp, nông nghiệp và cả những điều giản dị nhất.
Hãy thử nhìn quanh xem, có gì mà không có bóng dáng của phi kim? Oxi – dĩ nhiên rồi, không khí chúng ta hít thở chính là nguồn sống từ Oxi. Trong y tế, Oxi tinh khiết là thứ không thể thiếu để hỗ trợ hô hấp cho bệnh nhân. Công nghiệp cần Oxi cho các quá trình đốt cháy, hàn cắt kim loại.

Còn Nito thì sao? Chiếm phần lớn không khí, Nito lỏng siêu lạnh được dùng để bảo quản mẫu vật sinh học, trong y tế để điều trị da liễu. Trong công nghiệp thực phẩm, Nito được bơm vào bao bì để giữ cho sản phẩm tươi ngon lâu hơn. Quan trọng nhất, Nito là nguyên liệu chính để sản xuất amoniac, từ đó tạo ra phân bón cho nông nghiệp, giúp cây cối xanh tốt, cho ra mùa màng bội thu.
Đến lượt Lưu huỳnh, nghe có vẻ không mấy "thơm tho" nhưng lại cực kỳ quyền lực. Lưu huỳnh là nguyên liệu chính để sản xuất axit sulfuric (H₂SO₄) – được mệnh danh là "máu" của ngành công nghiệp hóa chất, dùng trong sản xuất phân bón, chất tẩy rửa, giấy, sơn, và vô số thứ khác. Lưu huỳnh còn giúp lưu hóa cao su, làm cho lốp xe bền và đàn hồi hơn.
Clo lại gắn liền với sự sạch sẽ. Bạn có nhận ra mùi đặc trưng ở bể bơi hay nước máy không? Đó chính là Clo đang làm nhiệm vụ khử trùng, tiêu diệt vi khuẩn, mang lại nguồn nước an toàn cho chúng ta. Ngoài ra, Clo là thành phần quan trọng trong sản xuất nhựa PVC, dung môi và nhiều hóa chất công nghiệp khác.
Cuối cùng, không thể không nhắc đến Carbon – nền tảng của mọi sự sống trên Trái Đất. Từ nhiên liệu hóa thạch chúng ta đốt hàng ngày (than, dầu mỏ) đến kim cương lấp lánh hay than chì trong bút chì, tất cả đều là Carbon. Trong công nghiệp, Carbon là thành phần chính để sản xuất thép, vật liệu lọc nước (than hoạt tính), và vô vàn hợp chất hữu cơ khác.
Nhìn xem, từ việc duy trì sự sống, sản xuất lương thực, làm sạch nước, chế tạo vật liệu, đến năng lượng chúng ta sử dụng, phi kim đều đóng vai trò then chốt. Chúng không phô trương như vàng bạc, nhưng lại là những viên gạch nền tảng xây dựng nên thế giới hiện đại và duy trì sự sống của chúng ta.
