Nhìn quanh mình xem, tất cả mọi thứ, từ cái bàn bạn đang ngồi đến không khí bạn hít thở, đều được tạo nên từ những viên gạch nhỏ bé. Trong thế giới hóa học, những viên gạch cơ bản nhất, chỉ được làm từ một loại nguyên tử duy nhất, được gọi là đơn chất. Như câu nói quen thuộc ‘Vàng thật không sợ lửa’, vàng chính là một ví dụ điển hình của đơn chất kim loại. Nhưng bạn có bao giờ tự hỏi, tại sao vàng lại rắn chắc, trong khi khí oxy chúng ta hít thở lại là chất khí, dù cả hai đều là đơn chất? Làm sao chúng ta biểu diễn chúng bằng công thức hóa học, và điều gì khiến đơn chất khác biệt hoàn toàn với hợp chất? Hãy cùng nhau giải mã những bí ẩn đằng sau khái niệm, cấu tạo và cách phân loại thú vị của đơn chất nhé!
Đơn chất Định nghĩa và bản chất đơn giản
Bạn đã bao giờ tự hỏi những viên kim loại sáng bóng hay khí bạn hít thở được tạo nên từ đâu chưa? Trong thế giới hóa học đầy màu sắc, chúng ta bắt gặp vô vàn loại chất khác nhau. Nhưng để hiểu sâu hơn, chúng ta cần bắt đầu từ những viên gạch cơ bản nhất, và đơn chất chính là một trong số đó.
Nói một cách dễ hiểu nhất, đơn chất là những chất được tạo nên từ chỉ một nguyên tố hóa học duy nhất. Tưởng tượng mỗi nguyên tố như một loại "nguyên liệu" đặc biệt (sắt, oxy, vàng…). Khi bạn chỉ dùng một loại nguyên liệu đó để xây dựng nên một "vật thể" (chất), thì "vật thể" đó chính là đơn chất.
Bản chất cốt lõi của đơn chất nằm ở sự "đơn giản" trong cấu tạo nguyên tố của nó. Dù các nguyên tử của nguyên tố đó có liên kết với nhau theo cách nào đi chăng nữa (chúng ta sẽ nói kỹ hơn ở phần sau), thì tất cả các nguyên tử cấu thành nên đơn chất đó đều thuộc về cùng một "gia đình" nguyên tố. Ví dụ, dù là khí oxy (O₂) hay ozon (O₃), chúng đều được tạo thành từ các nguyên tử oxy (O), nên cả hai đều là đơn chất của nguyên tố oxy.
Việc nắm vững định nghĩa và bản chất này cực kỳ quan trọng. Nó là nền tảng đầu tiên để chúng ta phân loại các chất trong hóa học. Thay vì nhìn vào hàng triệu chất khác nhau, chúng ta có thể chia chúng thành hai nhóm lớn dựa trên cấu tạo nguyên tố: đơn chất (chỉ từ một nguyên tố) và một nhóm khác phức tạp hơn (từ hai nguyên tố trở lên). Sự phân loại cơ bản này giúp chúng ta hệ thống hóa kiến thức và dễ dàng nghiên cứu tính chất của từng loại chất hơn rất nhiều.
Bên trong đơn chất Cấu trúc và phân loại hấp dẫn
Bạn có bao giờ tự hỏi, tại sao sắt lại cứng và dẫn điện tốt, trong khi oxy lại là chất khí không màu, không mùi? Bí mật nằm ngay ở cách các nguyên tử "bắt tay" nhau và sắp xếp bên trong mỗi loại đơn chất đấy. Cấu trúc nội tại này không chỉ quyết định tính chất, mà còn là cơ sở để chúng ta phân loại chúng một cách rành mạch.

Hãy thử tưởng tượng các nguyên tử như những viên bi tí hon. Với đơn chất kim loại, các viên bi này được xếp chồng lên nhau một cách cực kỳ gọn gàng và khít khao, tạo thành một mạng lưới không gian bền vững. Chúng liên kết với nhau bằng một kiểu "bắt tay" đặc biệt gọi là liên kết kim loại, nơi các electron có thể di chuyển khá tự do khắp mạng lưới. Chính cấu trúc "đông đúc" và sự di chuyển dễ dàng của electron này làm cho kim loại thường có vẻ ngoài sáng bóng, dễ kéo sợi hay dát mỏng, và đặc biệt là dẫn điện, dẫn nhiệt "đỉnh của chóp".
Ngược lại, đơn chất phi kim lại có cách sắp xếp "thoáng đãng" hơn nhiều. Các nguyên tử phi kim không đứng một mình hay xếp thành mạng lưới khổng lồ như kim loại. Thay vào đó, chúng thường liên kết với một số lượng nguyên tử nhất định của chính nó để tạo thành các nhóm nhỏ hơn gọi là phân tử. Ví dụ, oxy chúng ta hít thở không phải là nguyên tử O đứng riêng lẻ, mà là phân tử O₂ gồm hai nguyên tử O liên kết với nhau. Lưu huỳnh thì phức tạp hơn, có thể tồn tại dưới dạng phân tử S₈. Các phân tử này sau đó tồn tại độc lập hoặc liên kết yếu với nhau. Chính vì cấu trúc phân tử này mà phi kim thường tồn tại ở nhiều trạng thái khác nhau (rắn, lỏng, khí) và đa số là chất cách điện, cách nhiệt kém.
Còn một nhóm "đặc biệt" nữa là đơn chất khí hiếm. Các anh chàng này cực kỳ "độc lập". Mỗi "viên bi" nguyên tử đứng một mình, không thèm bắt tay với bất kỳ nguyên tử nào khác của nó cả. Cấu hình electron của chúng đã quá "ổn định" rồi, nên chẳng cần phải liên kết gì thêm cho mất công. Vì thế, khí hiếm luôn tồn tại dưới dạng các nguyên tử riêng lẻ và là chất khí ở nhiệt độ phòng, cực kỳ trơ về mặt hóa học.
Tóm lại, chỉ cần nhìn vào cách các nguyên tử "dàn trận" bên trong, chúng ta đã có thể phân biệt và hiểu được tại sao kim loại lại khác phi kim và khí hiếm đến vậy. Cấu trúc là chìa khóa để mở cánh cửa hiểu về tính chất của từng loại đơn chất này.
Công thức đơn chất Viết sao cho chuẩn
Khi nói đến hóa học, mỗi chất đều có một cách riêng để "giới thiệu" bản thân qua công thức hóa học. Đơn chất cũng vậy, chúng có những quy tắc biểu diễn riêng, tùy thuộc vào bản chất "tính cách" của nguyên tố tạo nên chúng.
Bạn biết đấy, đơn chất được tạo nên từ chỉ một loại nguyên tố. Nhưng cách các nguyên tử của nguyên tố đó "bắt tay" nhau lại không giống nhau. Chính sự khác biệt này dẫn đến cách viết công thức hóa học khác nhau cho các loại đơn chất.
Với những anh chàng kim loại như sắt (Fe), đồng (Cu), nhôm (Al) hay vàng (Au), các nguyên tử của chúng thường sắp xếp khít nhau tạo thành một mạng lưới khổng lồ. Không có "phân tử" riêng lẻ cụ thể nào ở đây cả. Vì thế, để biểu diễn đơn chất kim loại, người ta chỉ cần dùng ký hiệu hóa học của nguyên tố đó là đủ. Đơn giản mà hiệu quả!
Ví dụ nhé:
- Đơn chất sắt được viết là Fe.
- Đơn chất đồng là Cu.
- Đơn chất natri là Na.
Thế còn các "cô nàng" phi kim thì sao? À, các đơn chất phi kim lại hay "tụ tập" thành từng nhóm nhỏ có số lượng nguyên tử nhất định, tạo thành các phân tử riêng biệt. Số lượng nguyên tử trong mỗi phân tử này là cố định. Do đó, công thức hóa học của đơn chất phi kim cần phải thể hiện rõ điều này bằng cách sử dụng công thức phân tử, tức là có thêm chỉ số ở chân ký hiệu nguyên tố.
Chẳng hạn:
- Khí oxi mà chúng ta hít thở không phải là O đơn lẻ, mà là phân tử gồm 2 nguyên tử oxi liên kết với nhau, nên công thức là O₂.
- Khí nitơ trong không khí cũng vậy, là phân tử N₂, công thức là N₂.
- Khí hydro là H₂.
- Khí clo là Cl₂.
- Lưu huỳnh tồn tại dưới dạng phân tử có tới 8 nguyên tử, công thức là S₈.
- Phốt pho trắng là phân tử có 4 nguyên tử, công thức là P₄.
Còn một nhóm đặc biệt nữa là các khí hiếm (như Heli, Neon, Argon). Các nguyên tử khí hiếm rất "độc lập", chúng tồn tại riêng lẻ từng nguyên tử một. Vì vậy, công thức hóa học của đơn chất khí hiếm cũng giống như kim loại, chỉ cần dùng ký hiệu hóa học của nguyên tố đó.
Ví dụ:
- Đơn chất Heli là He.
- Đơn chất Neon là Ne.
- Đơn chất Argon là Ar.
Nắm vững cách biểu diễn công thức hóa học của đơn chất không chỉ giúp bạn viết đúng mà còn ngầm hiểu được cấu tạo và bản chất của chúng đấy. Đây là một trong những viên gạch đầu tiên cực kỳ quan trọng khi bước chân vào thế giới hóa học đầy thú vị!
Đơn chất và Hợp chất Nhận diện nhanh
Bạn biết không, thế giới vật chất quanh ta muôn hình vạn trạng, nhưng xét về mặt hóa học, chúng ta có thể chia chúng thành hai nhóm lớn cực kỳ quan trọng: đơn chất và hợp chất. Nắm vững cách phân biệt hai anh bạn này là coi như bạn đã có trong tay chìa khóa để mở cánh cửa hóa học rồi đấy!
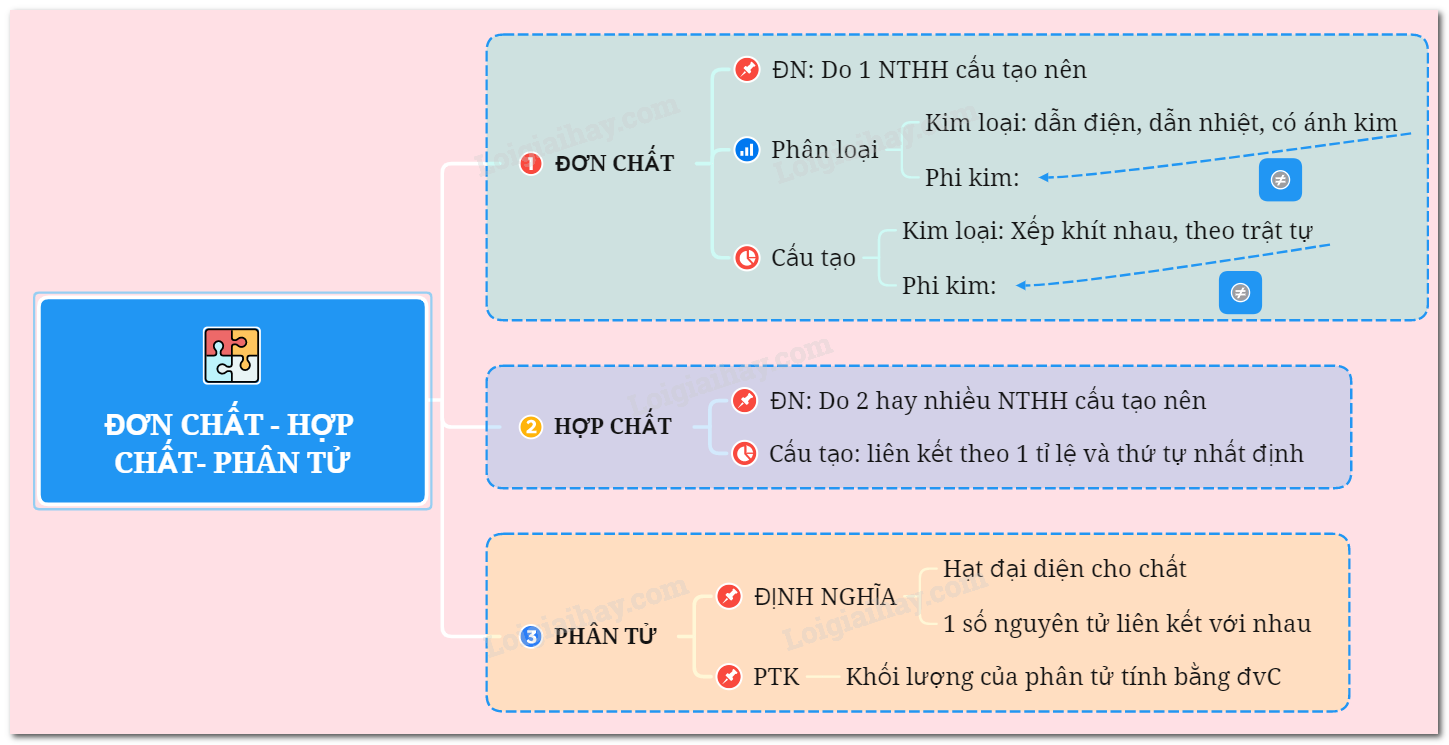
Điểm khác biệt đầu tiên, dễ nhận thấy nhất, nằm ngay ở cái tên. Đơn chất đúng như tên gọi, được tạo nên từ chỉ một loại nguyên tố hóa học duy nhất. Bạn cứ hình dung nó giống như một đội bóng mà tất cả cầu thủ đều là anh em sinh đôi vậy đó. Dù có thể có nhiều "cầu thủ" (nguyên tử) trong đội, nhưng tất cả đều cùng một "dòng họ" (nguyên tố).
Còn hợp chất thì sao? À, hợp chất phức tạp hơn một chút. Nó là sự kết hợp của hai hay nhiều loại nguyên tố hóa học khác nhau, liên kết với nhau theo một tỉ lệ xác định. Giống như một đội bóng đa quốc gia, mỗi cầu thủ đến từ một nơi khác nhau, cùng nhau tạo nên một tập thể mới.
Cách các nguyên tử "bắt tay" nhau cũng là điểm phân biệt rõ rệt. Trong đơn chất kim loại, các nguyên tử thường sắp xếp khít lại với nhau như một khối vững chắc. Đơn chất phi kim có thể tồn tại dưới dạng phân tử gồm vài nguyên tử cùng loại liên kết lại (như O₂ hay S₈). Còn trong hợp chất, các nguyên tử của các nguyên tố khác nhau sẽ liên kết với nhau bằng các loại liên kết hóa học đặc trưng để tạo thành phân tử hoặc mạng lưới tinh thể hoàn toàn mới.
Và đây là điểm mấu chốt khiến đơn chất và hợp chất hoàn toàn khác biệt: tính chất của chúng. Tính chất của đơn chất chính là tính chất đặc trưng của nguyên tố tạo ra nó. Ví dụ, sắt là đơn chất kim loại, nó có tính dẻo, dẫn điện, dẫn nhiệt. Oxi là đơn chất phi kim, nó là chất khí duy trì sự cháy.
Ngược lại, tính chất của hợp chất hoàn toàn khác biệt so với tính chất của các nguyên tố cấu thành nên nó. Lấy ví dụ kinh điển là nước (H₂O). Nước là chất lỏng ở điều kiện thường, dùng để dập lửa. Nhưng nó được tạo thành từ hydro (H₂) – một khí rất dễ cháy, và oxi (O₂) – một khí duy trì sự cháy. Bạn thấy không, khi kết hợp lại, chúng tạo ra một chất mới với tính chất hoàn toàn khác biệt và không thể đoán trước chỉ dựa vào tính chất của hydro và oxi riêng lẻ.
Chính nhờ những khác biệt rõ ràng về số lượng nguyên tố, cách liên kết và tính chất này mà chúng ta có thể dễ dàng phân loại các chất trong hóa học. Chỉ cần nhìn vào thành phần và cấu trúc, bạn sẽ biết ngay đó là đơn chất hay hợp chất, từ đó hiểu rõ hơn về bản chất và hành vi của chúng trong các phản ứng hóa học. Nắm chắc điều này, việc học hóa của bạn sẽ trở nên nhẹ nhàng và thú vị hơn rất nhiều đấy!
Đơn Chất Quanh Ta: Ví Dụ Và Ý Nghĩa Học Tập
Bắt đầu hành trình khám phá hóa học, chúng ta sẽ gặp những "ngôi sao" đầu tiên, đó chính là đơn chất. Nghe có vẻ xa lạ, nhưng thực ra chúng hiện diện quanh ta mỗi ngày đấy! Việc nhận diện và hiểu về đơn chất cực kỳ quan trọng, nó giống như việc bạn học bảng chữ cái trước khi đọc sách vậy.
Thử nghĩ xem, bạn có thấy những vật dụng bằng sắt (Fe) hay đồng (Cu) không? Cái cổng nhà vững chãi làm bằng sắt, hay những sợi dây điện dẫn khắp nhà bằng đồng. Đó chính là những ví dụ điển hình nhất về đơn chất kim loại. Chúng chỉ được tạo thành từ duy nhất một loại nguyên tử (nguyên tử sắt hoặc nguyên tử đồng), thường có vẻ ngoài sáng bóng đặc trưng và khả năng dẫn điện, dẫn nhiệt "đỉnh của chóp".
Còn không khí chúng ta hít thở thì sao? Dù là hỗn hợp, nhưng thành phần chính có một đơn chất cực kỳ thiết yếu: Oxi (O₂). Oxi là một đơn chất phi kim, được tạo thành từ hai nguyên tử O liên kết với nhau tạo thành phân tử O₂. Hay bạn có biết lưu huỳnh (S) không? Nó có màu vàng đặc trưng, thường xuất hiện ở các vùng núi lửa hoặc được dùng trong sản xuất diêm. Lưu huỳnh cũng là một đơn chất phi kim đấy. Khác với kim loại, phi kim thường không dẫn điện (trừ than chì), và có thể tồn tại ở dạng phân tử với số lượng nguyên tử khác nhau (như O₂ có 2 nguyên tử O, hay lưu huỳnh có thể tồn tại ở dạng S₈).
Nhẹ nhàng và "ít nói" hơn là các khí hiếm. Bạn có thấy những quả bóng bay bơm khí Heli (He) lơ lửng trên trời không? Hay những biển quảng cáo rực rỡ sắc màu nhờ khí Neon (Ne)? Heli và Neon là những đơn chất khí hiếm. Đặc điểm của chúng là các nguyên tử tồn tại độc lập, rất khó tham gia phản ứng hóa học với các chất khác.
Vậy tại sao việc "làm quen" với những ví dụ này và nắm vững khái niệm đơn chất lại quan trọng đến thế trong chương trình hóa học phổ thông? Đơn giản là vì đơn chất chính là nền tảng, là "viên gạch" đầu tiên để bạn xây dựng kiến thức hóa học của mình.
- Hiểu đơn chất giúp bạn dễ dàng phân biệt chúng với hợp chất – những chất được tạo thành từ nhiều loại nguyên tố khác nhau.
- Nó là cơ sở để bạn học về phản ứng hóa học, nơi các đơn chất có thể tham gia hoặc được tạo ra.
- Khi học sâu hơn về bảng tuần hoàn, cấu tạo nguyên tử, hay các bài toán tính toán hóa học phức tạp, kiến thức về đơn chất sẽ luôn là điểm tựa vững chắc giúp bạn hiểu rõ bản chất của vấn đề.
Nắm chắc khái niệm đơn chất và các ví dụ quen thuộc này, bạn đã có trong tay chiếc chìa khóa đầu tiên để mở cánh cửa vào thế giới hóa học đầy màu sắc và thú vị rồi đấy!
